Durante a reação de PCR, alguns fatores interferentes são frequentemente encontrados.
Devido à altíssima sensibilidade da PCR, a contaminação é considerada um dos fatores mais importantes que afetam os resultados da PCR e pode produzir resultados falso-positivos.
Igualmente importantes são as diversas fontes que levam a resultados falso-negativos. Se uma ou mais partes essenciais da mistura de PCR ou da própria reação de amplificação forem inibidas ou sofrerem interferência, o ensaio diagnóstico pode ser prejudicado. Isso pode levar à redução da eficiência e até mesmo a resultados falso-negativos.
Além da inibição, a perda da integridade do ácido nucleico alvo pode ocorrer devido às condições de transporte e/ou armazenamento antes do preparo da amostra. Em particular, altas temperaturas ou armazenamento inadequado podem levar a danos às células e aos ácidos nucleicos. A fixação de células e tecidos e a inclusão em parafina são causas bem conhecidas de fragmentação do DNA e um problema persistente (ver Figuras 1 e 2). Nesses casos, mesmo o isolamento e a purificação ideais não serão suficientes.
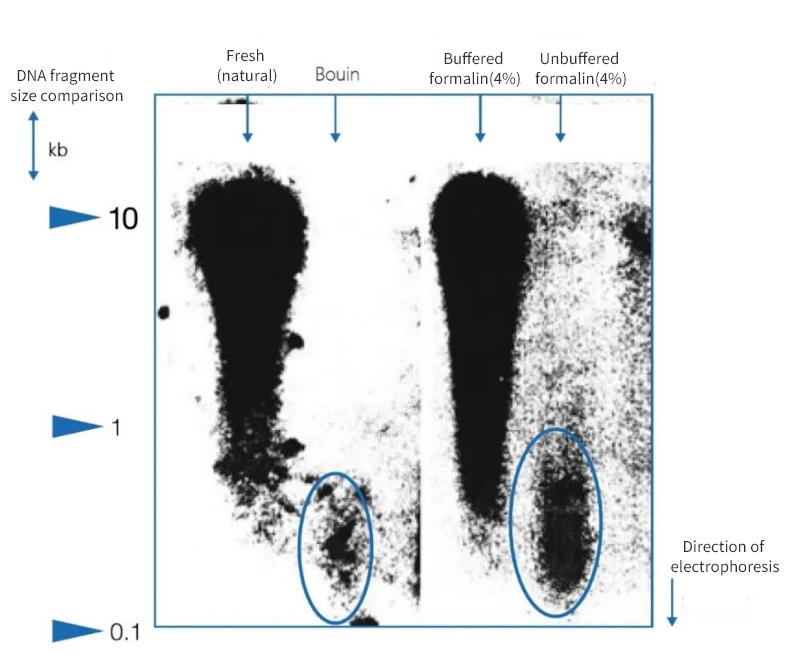
Figura 1 | Efeito da imobilização na integridade do DNA
A eletroforese em gel de agarose mostrou que a qualidade do DNA isolado de cortes de parafina de autópsias variava consideravelmente. Fragmentos de DNA com diferentes comprimentos médios estavam presentes nos extratos, dependendo do método de fixação. O DNA foi preservado apenas quando fixado em amostras congeladas nativas e em formalina neutra tamponada. O uso de um fixador de Bouin fortemente ácido ou de formalina não tamponada contendo ácido fórmico resultou em perda significativa de DNA. A fração restante está altamente fragmentada.
À esquerda, o comprimento dos fragmentos é expresso em pares de quilobases (kbp).
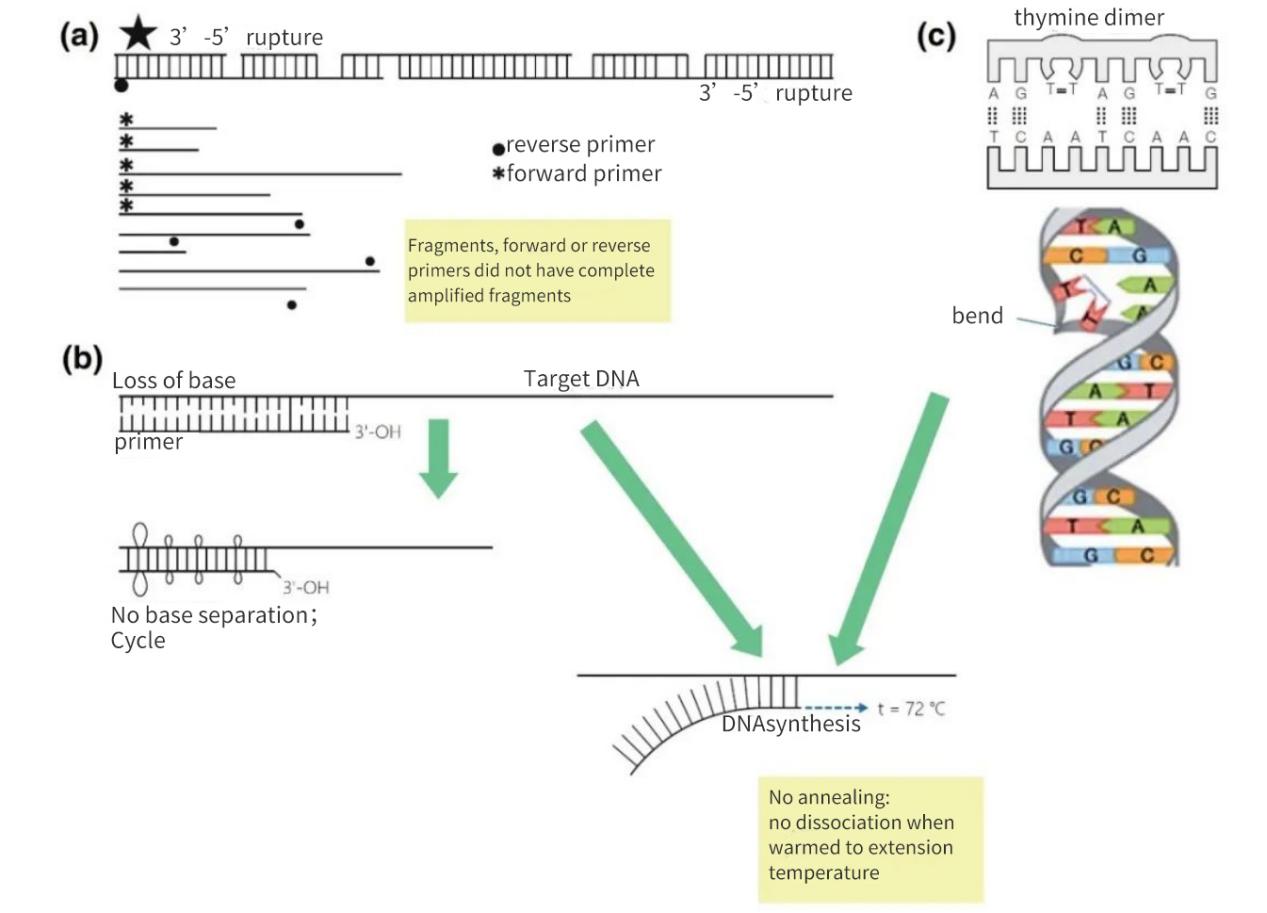
Figura 2 | Perda de integridade de alvos de ácido nucleico
(a) Uma lacuna de 3′-5′ em ambas as fitas resultará em uma quebra no DNA alvo. A síntese de DNA ainda ocorrerá no pequeno fragmento. No entanto, se um sítio de hibridização do primer estiver ausente no fragmento de DNA, ocorrerá apenas amplificação linear. No caso mais favorável, os fragmentos podem se resaturar mutuamente, mas os rendimentos serão baixos e abaixo dos níveis de detecção.
(b) A perda de bases, principalmente devido à despurinação e à formação de dímeros de timidina, leva a uma diminuição no número de ligações de hidrogênio e a uma diminuição na Tm. Durante a fase de aquecimento prolongado, os primers se desprendem do DNA da matriz e não se anelam mesmo em condições menos rigorosas.
(c) As bases de timina adjacentes formam um dímero TT.
Outro problema comum que frequentemente ocorre em diagnósticos moleculares é a liberação subótima de ácidos nucleicos alvo em comparação com a extração por fenol-clorofórmio. Em casos extremos, isso pode estar associado a resultados falso-negativos. Muito tempo pode ser economizado com a lise por fervura ou a digestão enzimática de detritos celulares, mas esse método geralmente resulta em baixa sensibilidade da PCR devido à liberação insuficiente de ácidos nucleicos.
Inibição da atividade da polimerase durante a amplificação
De forma geral, a inibição é usada como um conceito abrangente para descrever todos os fatores que levam a resultados subótimos na PCR. Em um sentido estritamente bioquímico, a inibição se limita à atividade da enzima, ou seja, reduz ou impede a conversão do substrato em produto por meio da interação com o sítio ativo da DNA polimerase ou seu cofator (por exemplo, Mg2+ para a Taq DNA polimerase).
Componentes da amostra ou vários tampões e extratos contendo reagentes podem inibir diretamente a enzima ou aprisionar seus cofatores (por exemplo, EDTA), inativando assim a polimerase e, consequentemente, levando a resultados de PCR diminuídos ou falsos negativos.
No entanto, muitas interações entre os componentes da reação e os ácidos nucleicos que contêm o alvo também são designadas como 'inibidores de PCR'. Uma vez que a integridade da célula é rompida pelo isolamento e o ácido nucleico é liberado, podem ocorrer interações entre a amostra e a solução e a fase sólida circundantes. Por exemplo, 'sequestradores' podem se ligar ao DNA de fita simples ou dupla por meio de interações não covalentes e interferir no isolamento e na purificação, reduzindo o número de alvos que eventualmente chegam ao recipiente de reação da PCR.
De modo geral, os inibidores da PCR estão presentes na maioria dos fluidos corporais e reagentes utilizados em testes de diagnóstico clínico (ureia na urina, hemoglobina e heparina no sangue), em suplementos alimentares (componentes orgânicos, glicogênio, gordura, íons Ca2+) e em componentes do meio ambiente (fenóis, metais pesados).
| Inibidores | Fonte |
| Íons de cálcio | Leite, tecido ósseo |
| Colágeno | Tecido |
| Sais biliares | Fezes |
| Hemoglobina | No sangue |
| Hemoglobina | Amostras de sangue |
| Ácido húmico | Solo, planta |
| Sangue | Sangue |
| Lactoferrina | Sangue |
| (Europeia) melanina | Pele, cabelo |
| Mioglobina | Tecido muscular |
| Polissacarídeos | Planta, fezes |
| Protease | Leite |
| Ureia | Urina |
| Mucopolissacarídeo | Cartilagem, membranas mucosas |
| Lignina, celulose | Plantas |
Inibidores de PCR mais comuns podem ser encontrados em bactérias e células eucarióticas, DNA não alvo, macromoléculas de ligação ao DNA presentes em matrizes teciduais e equipamentos de laboratório, como luvas e plásticos. A purificação de ácidos nucleicos durante ou após a extração é o método preferido para a remoção de inibidores de PCR.
Atualmente, diversos equipamentos automatizados de extração podem substituir muitos protocolos manuais, mas a recuperação e/ou purificação de 100% dos alvos ainda não foi alcançada. Potenciais inibidores podem estar presentes nos ácidos nucleicos purificados ou já podem ter exercido seu efeito. Existem diferentes estratégias para reduzir o impacto dos inibidores. A escolha da polimerase adequada pode ter um impacto significativo na atividade do inibidor. Outros métodos comprovados para reduzir a inibição da PCR incluem o aumento da concentração da polimerase ou a aplicação de aditivos como a BSA.
A inibição das reações de PCR pode ser demonstrada pelo uso do controle de qualidade do processo interno (CIP).
É preciso ter cuidado para remover todos os reagentes e outras soluções do kit de extração, como etanol, EDTA, CETAB, LiCl, GuSCN, SDS, isopropanol e fenol, do isolado de ácido nucleico por meio de uma lavagem completa. Dependendo da concentração, essas substâncias podem ativar ou inibir a PCR.
Data da publicação: 19 de maio de 2023
 中文网站
中文网站