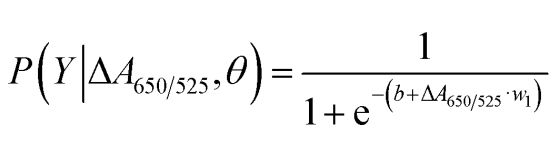A detecção precoce do câncer por meio de biópsia líquida é uma nova abordagem para o diagnóstico e detecção do câncer, proposta pelo Instituto Nacional do Câncer dos EUA nos últimos anos, com o objetivo de detectar o câncer em estágio inicial ou mesmo lesões pré-cancerosas. Tem sido amplamente utilizada como um novo biomarcador para o diagnóstico precoce de diversas neoplasias malignas, incluindo câncer de pulmão, tumores gastrointestinais, gliomas e tumores ginecológicos.
O surgimento de plataformas para identificar biomarcadores de perfil de metilação (Methylscape) tem o potencial de melhorar significativamente o rastreio precoce do câncer, colocando os pacientes no estágio mais inicial em que o tratamento é possível.
Recentemente, pesquisadores desenvolveram uma plataforma de detecção simples e direta para o mapeamento da metilação do DNA, baseada em nanopartículas de ouro decoradas com cisteamina (Cyst/AuNPs) combinadas a um biossensor integrado a um smartphone. Essa plataforma permite a triagem precoce e rápida de uma ampla gama de tumores. A triagem precoce para leucemia pode ser realizada em até 15 minutos após a extração do DNA de uma amostra de sangue, com uma precisão de 90%. O título do artigo é "Detecção rápida de DNA cancerígeno em sangue humano usando AuNPs revestidas com cisteamina e um smartphone com aprendizado de máquina".
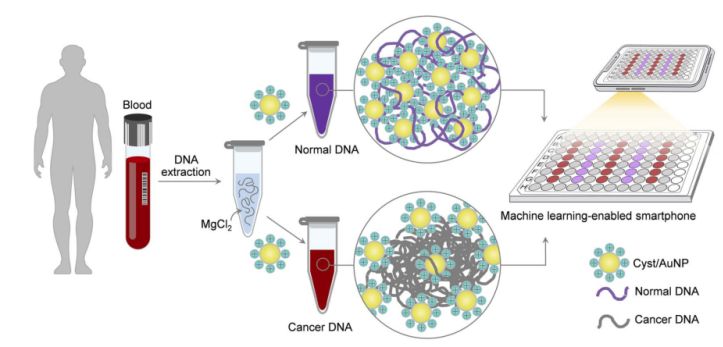
Figura 1. Uma plataforma de detecção simples e rápida para triagem de câncer por meio de componentes Cyst/AuNPs pode ser implementada em duas etapas simples.
Isso é ilustrado na Figura 1. Primeiramente, uma solução aquosa foi utilizada para dissolver os fragmentos de DNA. Em seguida, as Cyst/AuNPs foram adicionadas à solução. O DNA normal e o DNA maligno apresentam propriedades de metilação diferentes, resultando em fragmentos de DNA com padrões de auto-montagem distintos. O DNA normal forma agregados frouxos e, eventualmente, agrega as Cyst/AuNPs, o que resulta no deslocamento para o vermelho da coloração das Cyst/AuNPs, permitindo a observação da mudança de cor de vermelho para roxo a olho nu. Em contraste, o perfil de metilação único do DNA cancerígeno leva à formação de aglomerados maiores de fragmentos de DNA.
Imagens de placas de 96 poços foram obtidas usando a câmera de um smartphone. O DNA do câncer foi medido por um smartphone equipado com aprendizado de máquina, em comparação com métodos baseados em espectroscopia.
Rastreio de cancro em amostras de sangue reais
Para ampliar a utilidade da plataforma de detecção, os pesquisadores aplicaram um sensor que distinguiu com sucesso entre DNA normal e canceroso em amostras reais de sangue. Os padrões de metilação em sítios CpG regulam epigeneticamente a expressão gênica. Em quase todos os tipos de câncer, observou-se a alternância de alterações na metilação do DNA e, consequentemente, na expressão de genes que promovem a tumorigênese.
Como modelo para outros tipos de câncer associados à metilação do DNA, os pesquisadores utilizaram amostras de sangue de pacientes com leucemia e controles saudáveis para investigar a eficácia do perfil de metilação na diferenciação de cânceres leucêmicos. Esse biomarcador de perfil de metilação não apenas supera os métodos de triagem rápida de leucemia existentes, como também demonstra a viabilidade de sua aplicação na detecção precoce de uma ampla gama de cânceres utilizando esse ensaio simples e direto.
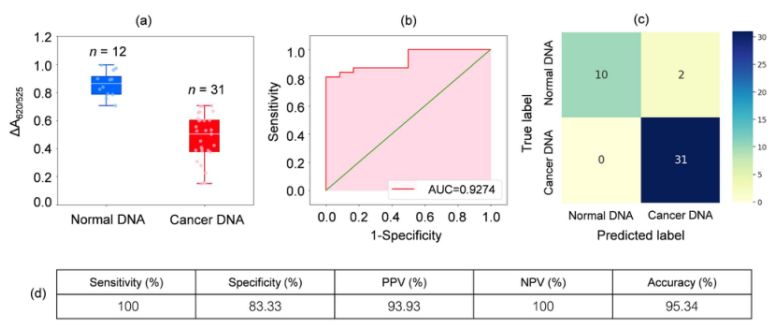
O DNA de amostras de sangue de 31 pacientes com leucemia e 12 indivíduos saudáveis foi analisado. Como mostrado no gráfico de caixa da Figura 2a, a absorbância relativa das amostras cancerígenas (ΔA650/525) foi menor do que a do DNA das amostras normais. Isso se deveu principalmente ao aumento da hidrofobicidade, levando à agregação densa do DNA cancerígeno, o que impediu a agregação das nanopartículas de ouro funcionalizadas com cisteína (Cyst/AuNPs). Como resultado, essas nanopartículas foram completamente dispersas nas camadas externas dos agregados cancerígenos, o que resultou em uma dispersão diferente das Cyst/AuNPs adsorvidas nos agregados de DNA normal e cancerígeno. As curvas ROC foram então geradas variando-se o limiar de um valor mínimo de ΔA650/525 a um valor máximo.
Figura 2.(a) Valores de absorbância relativa de soluções de cisto/AuNPs mostrando a presença de DNA normal (azul) e cancerígeno (vermelho) em condições otimizadas.
(DA650/525) de diagramas de caixa; (b) Análise ROC e avaliação de testes diagnósticos. (c) Matriz de confusão para o diagnóstico de pacientes normais e com câncer. (d) Sensibilidade, especificidade, valor preditivo positivo (VPP), valor preditivo negativo (VPN) e acurácia do método desenvolvido.
Como mostrado na Figura 2b, a área sob a curva ROC (AUC = 0,9274) obtida para o sensor desenvolvido apresentou alta sensibilidade e especificidade. Como pode ser observado no gráfico de caixa, o ponto mais baixo, representando o grupo de DNA normal, não está bem separado do ponto mais alto, representando o grupo de DNA cancerígeno; portanto, a regressão logística foi utilizada para diferenciar os grupos normal e cancerígeno. Dado um conjunto de variáveis independentes, estima-se a probabilidade de ocorrência de um evento, como um grupo cancerígeno ou normal. A variável dependente varia entre 0 e 1. O resultado é, portanto, uma probabilidade. Determinamos a probabilidade de identificação de câncer (P) com base em ΔA650/525 da seguinte forma.
onde b = 5,3533 e w1 = -6,965. Para a classificação das amostras, uma probabilidade inferior a 0,5 indica uma amostra normal, enquanto uma probabilidade igual ou superior a 0,5 indica uma amostra cancerosa. A Figura 2c apresenta a matriz de confusão gerada pela validação cruzada leave-it-alone, utilizada para validar a estabilidade do método de classificação. A Figura 2d resume a avaliação do teste diagnóstico do método, incluindo sensibilidade, especificidade, valor preditivo positivo (VPP) e valor preditivo negativo (VPN).
Biossensores baseados em smartphones
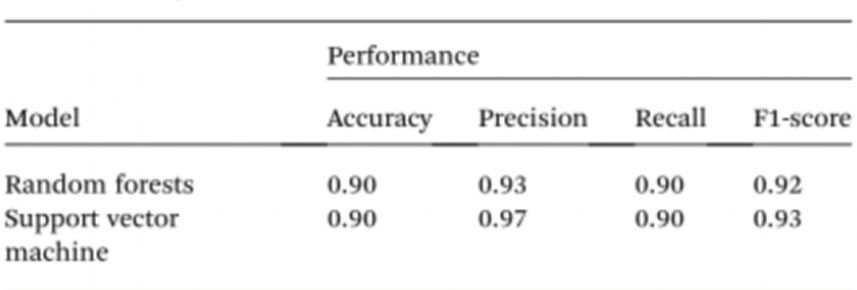
Para simplificar ainda mais a análise de amostras sem o uso de espectrofotômetros, os pesquisadores utilizaram inteligência artificial (IA) para interpretar a cor da solução e distinguir entre indivíduos normais e cancerosos. Para isso, a visão computacional foi usada para traduzir a cor da solução de Cyst/AuNPs em DNA normal (roxo) ou DNA canceroso (vermelho) a partir de imagens de placas de 96 poços capturadas pela câmera de um celular. A inteligência artificial pode reduzir custos e melhorar a acessibilidade na interpretação da cor de soluções de nanopartículas, sem a necessidade de acessórios ópticos para smartphones. Por fim, dois modelos de aprendizado de máquina, Random Forest (RF) e Support Vector Machine (SVM), foram treinados para construir os modelos. Ambos os modelos, RF e SVM, classificaram corretamente as amostras como positivas e negativas com uma precisão de 90%. Isso sugere que o uso de inteligência artificial em biossensores baseados em celulares é bastante viável.
Figura 3. (a) Classe alvo da solução registrada durante a preparação da amostra para a etapa de aquisição de imagem. (b) Exemplo de imagem obtida durante a etapa de aquisição de imagem. (c) Intensidade de cor da solução de cisto/AuNPs em cada poço da placa de 96 poços, extraída da imagem (b).
Utilizando Cyst/AuNPs, pesquisadores desenvolveram com sucesso uma plataforma de detecção simples para o mapeamento da metilação do DNA e um sensor capaz de distinguir DNA normal de DNA cancerígeno em amostras de sangue reais para triagem de leucemia. O sensor desenvolvido demonstrou que o DNA extraído de amostras de sangue reais foi capaz de detectar de forma rápida e econômica pequenas quantidades de DNA cancerígeno (3 nM) em pacientes com leucemia em 15 minutos, apresentando uma precisão de 95,3%. Para simplificar ainda mais a análise das amostras, eliminando a necessidade de um espectrofotômetro, o aprendizado de máquina foi utilizado para interpretar a cor da solução e diferenciar entre indivíduos normais e cancerígenos por meio de uma fotografia tirada com um celular, alcançando também uma precisão de 90,0%.
Referência: DOI: 10.1039/d2ra05725e
Data da publicação: 18/02/2023
 中文网站
中文网站